Популярные статьи

Светлана Чижова врач – дерматолог, косметолог «Центр лечебной косметологии Даная»
Тамара Корчевая врач-дерматолог, кандидат медицинских наук «Центр лечебной косметологии Даная»
Акне – это хроническое генетически обусловленное заболевание сальных желез, характеризующееся их повышенной активностью, которая формируется в ответ на стимуляцию их работы андрогенами, продуктами жизнедеятельности микроорганизмов, а также фолликулярным гиперкератозом и воспалительной реакцией тканей. Патология проявляется формированием на участках кожи, богатых сальными железами, невоспалительных и воспалительных элементов.
Локализация высыпаний на лице практически у всех пациентов приводит к возникновению у них психоэмоциональных нарушений – дисморфофобий и дисморфоманий. Несмотря на то, что акне не относится к ургентным состояниям, наличие угрей нередко является причиной появления тревоги, депрессии, а в некоторых случаях может привести и к суициду.
Основное значение в развитии aкне имеет наследственная предрасположенность. Так, вероятность возникновения акне у подростков в случае болезни обоих родителей составляет 50%. Причем чем тяжелее степень акне, тем чаще прослеживается генетическая взаимосвязь заболевания с патологией у ближайших родственников. Генетически передаются состояние гиперандрогении различного генеза, играющие ведущую роль в развитии акне.
Многообразные этиологические факторы, сложные патогенетические механизмы aкне и различные клинические формы заболевания способствовали появлению большого количества используемых методов лечения. Умелое сочетание разных препаратов для внутреннего и наружного применения позволяет получить хорошие результаты у большинства лиц, страдающих этим заболеванием.
Целью настоящего исследования явилась оптимизация терапии акне средней и тяжелой степени тяжести у женщин с яичниковой гиперандрогенией.
Высокий уровень заболеваемости акне в настоящее время делает актуальным исследование патогенеза этого дерматоза и поиск новых методов лечения. Сочетанное применение Роаккутана в малых дозах и комбинированного орального контрацептива Джес дает выраженный клинический эффект на фоне хорошей переносимости терапии.
ПРЕДМЕТ И МЕТОДЫ ИССЛЕДОВАНИЯ
В исследовании приняли участие 112 пациенток со средней и тяжелой формой папуло-пустулезного акне и яичниковой гиперандрогенией. Их средний возраст составил 26,45±7,17 лет, причем преобладали пациентки в возрасте от 19 до 30 лет (75%). В группу сравнения вошли 30 практически здоровых женщин соответствующего возраста.
Возраст появления первых признаков дерматоза в группе обследованных варьировался от 12 до 27 лет и в среднем составил 17,34±5,38 лет. Дебют акне у больных старше 25 был констатировался у 12 человек (10,71%). Длительность течения акне у пациенток варьировалась от нескольких месяцев до 15 лет и в среднем составила 6,16±5,38 лет.
Генеалогический анализ показал, что у 14 женщин (12,5%) акне страдали отцы, у 46 (41,07%) – матери, у 37(33,04%) – оба родителя. Лишь у 15 человек (13,39%) никто из родственников не перенес подобной патологии. Таким образом, преобладало количество пациенток с наследственной отягощенностью по линии матери. В зависимости от проводимого лечения пациентки были разделены на три группы.
- Первая группа включала 35 пациенток, которым была проведена комплексная терапия, подразумевающая использование стандартных средств наружного применения (после очищения кожи применяли гель с азелаиновой кислотой и/или гель с бензоилпероксидом и/или гель с адапаленом) и проем комбинированного орального контрацептива (КОК) Джес (этинилэстрадиол 0,02 мг, дроспиренон 3 мг). Были назначены 24 таблетки КОК и 4 таблетки плацебо. Лечение проводилось в течение 1 года.
- Вторая группа состояла из 38 женщин, которым была проведена монотерапия препаратом Роаккутан (изотретиноин) в дозе 0,5–1 мг/кг в течение 4–8 месяцев до достижения общей курсовой дозы 120мг/кг.
- Третья группа включала 39 больных, получавших комбинированную терапию с использованием препарата Роаккутан в дозе 10 мг в сутки в течение 6 месяцев и орального контрацептива Джес в течение 1 года.
Всем пациенткам было проведено ряд обследований, в частности дерматологический осмотр с определением индекса акне (ДИА), комплекс лабораторных и инструментальных тестов – исследование гормонального статуса, биохимический анализ крови, себуметрия, корнеометрия.
РЕЗУЛЬТАТЫ ИССЛЕДОВАНИЯ
Дерматологический индекс акне
Анализ динамики дерматологического индекса акне продемонстрировал эффективность проводимой терапии у всех больных.
В первой группе достоверное снижение средних значений ДИА наблюдалось к третьему месяцу лечения и составило 44,81%, к шестому месяцу – 64,14% к концу года – 66,84%.
Во второй группе динамика клинических симптомов была более интенсивной: через три месяца лечения средние значения ДИА снизились на 64,96%, через полгода – на 96,71% и через год – на 90,22%.
В третьей группе пациенток к третьему месяцу терапии наблюдалось достоверное снижение ДИА на 60,51%, через полгода – на 93,66% и через год – на 92,66%.
Клиническая ремиссия
В группах, где применялся Роаккутан, констатирована клиническая ремиссия, которая отмечалась при монотерапии этим препаратом у 94,74% больных, а при сочетании его с Джесом – у 92,31% пациенток. В первой же группе ремиссия наблюдалась лишь у 48,57% больных.
Переносимость и побочные реакции
Переносимость лечения в трех группах больных также была различной. В первой группе побочные реакции были зарегистрированы у 74,29% больных, в частности в 1–2-ой месяцы лекарственной терапии у 6 женщин (17,14%) отмечались межменструальные кровотечения. При проведении наружной терапии у 20 больных (57,14%) в первые три месяца лечения появлялись симптомы дерматита. Однако все нежелательные явления, возникающие у пациентов этой группы, разрешились примерно через 4 месяца после начала лечения. Во второй группе в результате приема Роаккутана в дозе 0,5–1,0 мг/кг нежелательные побочные явления отмечались у 100% больных и характеризовались формированием ретиноевого дерматита на коже лица, шеи, тыльных поверхностях кистей рук и локтевых сгибов. Кроме того, у всех пациенток возникал хейлит, а носовые кровотечения отмечались у 21,05% больных данной группы. В третьей группе побочные реакции наблюдались только у 28,02% пациенток и проявлялись в виде ретиноевого хейлита и незначительного шелушения кожи в области щек. Эти явления разрешились через 10–24 дня после начала приема ретиноида и не требовали отмены препарата. У 5,13% пациентов этой группы отмечались межменструальные кровотечения в первые 1–2 месяца приема контрацептива Джес. Таким образом, наиболее безопасным и эффективным методом лечения являлась комбинированная терапия с использованием Роаккутана и контрацептива Джес.
Гормональный статус
В первой группе пациентов отмечалась нормализация гормонального статуса и устранение признаков гиперандрогении. Средние значения лютеинизирующего гормона достоверно снизились с 15,77±0,99 до 7,43±0,73 мЕд/мл, нормализовались показатели гонадотропного индекса (ЛГ/ФСГ). Было отмечено достоверное снижение уровня общего и свободного тестостерона и соотношения Тобщ/Е2 до 10,81±1,08. Помимо этого было выявлено снижение уровня андростенона, а также 17-ОНП с 4,13±0,66 до 2,86±0,34 нмоль/л. При ультразвуковом исследовании было отмечено достоверное снижение объема яичников с 9,9±1,9 до 7,8±1,4 см3. У больных второй группы гормональный фон не изменился.
У пациенток третьей группы наблюдалось устранение гиперандрогении на фоне выраженных клинических результатов. Было отмечено снижение средних значений ЛГ более чем в 2 раза – с 16,21±1,53 до 6,35±0,75 мЕд/мл, что привело к депрессии соотношения ЛГ/ФСГ до 1,24±0,42. Помимо этого регистрировалось снижение концентрации общего тестостерона до 2,05±0,07 нмоль/л и соотношения Тобщ/Е2 до 8,35±3,26, что составило 50% от значений этого показателя до начала лечения. В результате проведенной терапии также наблюдалось понижение свободного тестостерона до 2,12±0,35 пг/мл, андростендиона до 10,02±1,99 нмоль/л, ДГЭА-С до 2,05±0,31 мкмоль/л и 17-ОНП до 1,75±0,25 нмоль/л.
При ультразвуковом исследовании у больных этой группы было зафиксировано уменьшение объема яичников с 10,2±0,54 до 6,24±0,1см3.
Биохимические показатели крови
У больных первой группы через шесть месяцев после начала лечения наблюдалось повышение показателя сывороточного железа до 25,37±1,02 мкмоль/л, однако уже к 12-му месяцу терапии он вернулся к нормальным значениям (21,46±4,21 мкмоль/л). В результате применения КОК у больных отмечалось достоверное снижение средних значений холестерина с 7,83±0,05 моль/л до 4,55±0,24 моль/л, повышение уровня липопротеидов высокой плотности с 0,96±0,02 моль/л до 1,52±0,08 моль/л, снижение средних значений липопротеидов низкой плотности с 4,37±0,28 моль/л до 1,63±0,09 моль/л. Таким образом, использование КОК при гиперандрогении у женщин с акне способствовало устранению дислипидемии, что оказало положительное влияние на работу сердечно-сосудистой системы у данного контингента больных.
Во второй группе отклонения в биохимическом анализе крови отмечались преимущественно к 6-му месяцу терапии, но они носили транзиторный характер и нормализовались к концу года. Увеличение показателей печеночных ферментов не превышало 50% от исходного уровня, что не является клинически значимым при использовании Роаккутана.
В третьей группе динамика изменений биохимических показателей не отличалась от таковой в первой. Было выявлено снижение уровня холестерина с 7,09±0,15 до 4,53±0,97 моль/л и повышение количества липопротеидов высокой плотности: через три месяца лечения с 0,99±0,03
моль/л до 1,35±0,03 моль/л и через полгода – до 1,34±0,03 моль/л с последующим некоторым понижением через год (до 1,01±0,002моль/л). Нормализация липидного обмена также была обусловлена снижением уровня ЛПНП – через 6 месяцев показатель уменьшился с 3,87±0,36 моль/л до 1,99±0,02 моль/л, и сохранялся на этом же уровне (1,98±0,03 моль/л) до конца года. Подобная тенденция отмечалась и при анализе динамики значений триглицеридов.
Таким образом, в первой и третьей группах наблюдалась нормализация липидного обмена, а во второй группе – повышение показателя печеночных ферментов, но не более чем в два раза с возвращением на уровень нормальных значений через 6 месяцев после отмены Роаккутана.
Себуметрия
В первой группе обследуемых через 6 месяцев после начала лечения количество больных с признаками гиперпродукции кожного сала уменьшилось на 45,71%. Через полгода после отмены контрацептива избыточное выделение себума наблюдалось лишь у 28,57% пациенток. Во второй группе через 6 месяцев после начала лечения у 55,26%, больных отмечалась выраженная сухость кожи лица и у 44,74% женщин – нормальное салоотделение. Через год после начала лечения и через 4–6 месяцев после окончания терапии во второй группе себорея была констатирована только у 2,86%, что иллюстрирует выраженное противорецидивное действие данного метода. В третьей группе также был отмечен себостатический эффект комбинированной терапии: выявлено снижение количества пациенток с себореей через полгода на 71,79% (с 82,05% до 10,26%). Себуметрия, выполненная через год после начала лечения, продемонстрировала повышение продукции кожного сала только у 7,69% женщин, причем ксероза кожи выявлено не было (рис. 1).
Корнеометрия
В первой группе, через 6 месяцев после начала лечения у 60% пациенток отмечалось уменьшение увлажненности кожи, тогда как у 40% больных этот показатель оставался в норме. Через полгода после отмены наружного лечения обезвоженность кожи отмечалась только у 8,57% женщин. Во второй группе применение Роаккутана в стандартных дозах способствовало выраженной потере влаги у 52,63% больных и формированию обезвоженности кожи у 47,37% пациентов. Через год после начала лечения обезвоженность кожи отмечалась у 28,95%, нормальная увлажненность – у 71,05% больных. То есть после отмены Роаккутана происходила нормализация функции эпидермального барьера с уменьшением трансэпидермальной потери воды. Применение комбинации Роаккутана в низких дозах и контрацептива Джес наименее всего влияло на потерю влаги во время лечения: через полгода терапии соотношение пациенток с обезвоженной кожей и нормально увлажненной составило 23,08% к 76,92% и через год – 12,82% к 87,18% соответственно .
ЗАКЛЮЧЕНИЕ
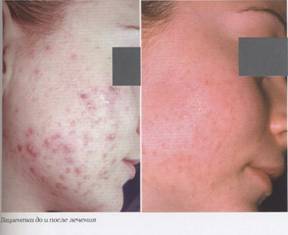
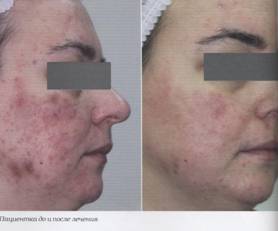
Нередко повышение эффективности проводимой терапии акне сопровождается увеличением частоты возникновения нежелательных реакций. В настоящем исследовании было доказано, что комбинированное лечение с использованием Роаккутана в суточной дозе 10 мг и орального контрацептива нового поколения Джес способствует не только формированию выраженного клинического результата, но и обуславливает низкую вероятность возникновения побочных явлений. Результаты проведенного лечения представлены на фото.
Пациентка до и после лечения Пациентка до и после лечения
Рекомендуемая литература
1. Аравийская Е.Р. «Современный взгляд на лечение акне: состояние проблемы и новые возможности». «Лечащий врач», 2003, стр 4.
2. Иванов О.Л., Самгин М.А. «Антиандрогенные препараты: современная терапия акне у женщин». «Гинекология», №5, 2005, том 11.
3. Кубанова А.А., Самсонов В.А., Забненкова О.В. «Современные особенности патогенеза и терапии акне». «Вестник дерматологии и венерологии». 2003, №1, стр. 9–16.
4. Полонская Н.А. «Угревая болезнь: классификация, патогенез, лечение». Статья из оn-line еженедельника, 2002.
5. Самгин М.А., Монахов С.А. «Новое в патогенезе и местной терапии угревой сыпи» «Вестник дерматологии и венерологии», №2, 2003, стр. 31–38. 6. Cunliffe W.J. et al. Current concepts in the treatment of acne vulgar. Simposium at the EADV 12.10.2000 Geneva. Geneva, 2000.
7. Jacyk W.K. Adapalen in the treatment of African patients. J. Eur. Acad. Dermatol. Venereol. 2001, 15, suppl.3, рр. 37–42.
8. Katz H.I. Effect of a desogestrel-containing oral contraceptive on the skin. The European Journal of Contraception and Reproductive Health Care. 2000, vol. 5, № 4, рр. 83–110.
9. Thiboutot D. New treatment and therapeutic strategies for acne. Arch. Fam. Med., 2000, 9, рр. 179–187.
10. Thiboutot D.M. Endocrinological evaluation and hormonal therapy for women with difficult acne. J. Eur. Acad. Dermatol. Venereol. 2001, 15, suppl.3, рр. 57–61.
11. Zouboulis C.C., Eady A., Philpott M., Goldsmith L.A., Orfanos C., Cunliffe W.C., Rosenfield R. What is the pathogenesis of acne? Experimental dermatology 2005,14(2),143–52.

